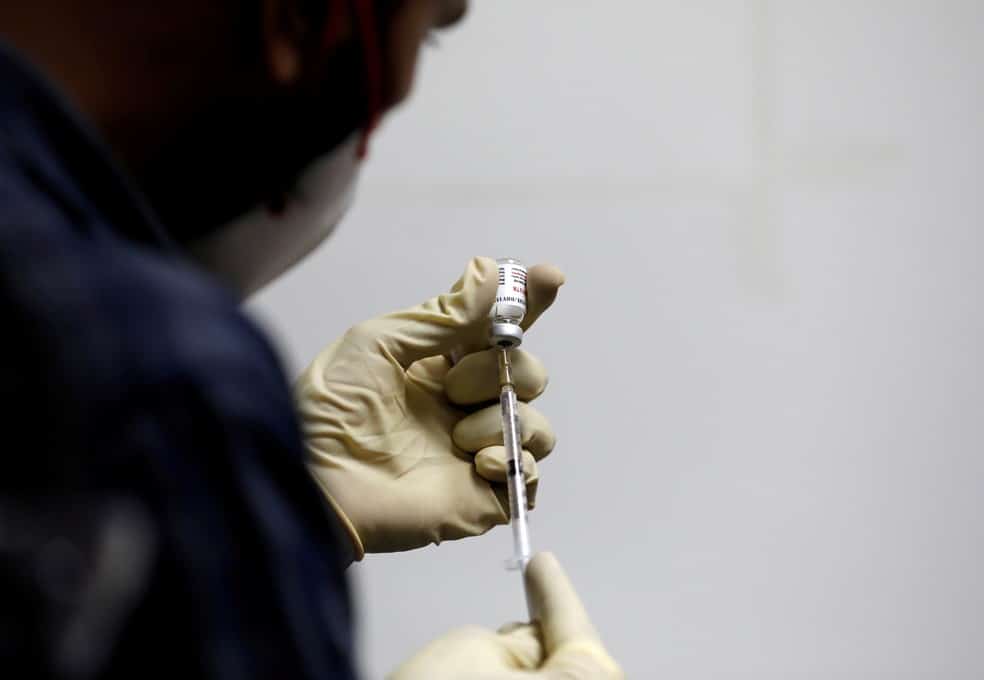
A Agência, que havia rejeitado a compra dos imunizantes, mudou a orientação depois da chegada de novos documentos das fabricantes. Diante da crise sanitária, a Agência autorizou a importação do imunizantes com restrições
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, nesta sexta-feira (4), o pedido de importação excepcional das vacinas Sputnik V e Covaxin contra a Covid-19. (Veja abaixo o que significa a decisão da Agência).
A Agência, que havia rejeitado a importação dos imunizantes, mudou a orientação depois da chegada de novos documentos das fabricantes. Ainda assim, estabeleceu protocolos específicos para aplicação das doses e limitação de público que pode ser vacinado.
Covaxin e Sputnik V: O que muda na vacinação do Brasil com decisão da Anvisa
A Sputnik V foi requisitada por seis estados: Bahia, Maranhão, Sergipe, Ceará, Pernambuco e Piauí. Em abril, um pedido de 30 milhões de doses para 14 estados foi rejeitado pela Anvisa.
A Covaxin faz parte de encomenda do Ministério da Saúde, que renovou o pedido de importação de 20 milhões de doses – em março, a compra também foi negada pela agência.
A Anvisa já aprovou para uso no Brasil a CoronaVac, a vacina de Oxford/AstraZeneca, a da Pfizer/BioNTech e a da Johnson. Esta última, entretanto, ainda não tem doses disponíveis no país.
Veja abaixo, para entender de forma mais detalhada, as principais perguntas sobre as duas vacinas:
- Quais vacinas estavam em análise?
- A Anvisa autorizou o uso emergencial dessas vacinas?
- Mas as doses importadas poderão ser usadas?
- Quais são as condições impostas pela Anvisa?
- Em quais casos as doses dessas vacinas não poderão ser aplicadas?
- Serão quantas doses importadas?
- As doses serão entregues ao Progama Nacional de Imunizações (PNI)?
- O uso pode ser suspenso?
Quais vacinas estavam em análise?
Estavam em análise dois pedidos:
- importação de doses da Covaxin pelo Ministério da Saúde
- importação de doses da Sputnik V pelos estados
O pedido de importação pelos estados é distinto e independente do pedido de uso emergencial feito pela União Química, que produz a Sputnik V no Brasil. O pedido da União Química está com prazo de análise suspenso e depende de informações completas do laboratório — que serão analisadas separadamente pela Anvisa.
A Anvisa autorizou o uso emergencial dessas vacinas?
Não. A agência autorizou a importação em caráter excepcional dos lotes solicitados. Ou seja, outros lotes da Covaxin e Sputnik V só poderiam chegar ao Brasil caso esse mesmo pedido à Anvisa fosse refeito.
As farmacêuticas teriam de fazer uma outra solicitação se quiserem a autorização do uso emergencial desses imunizantes, o que permitiria a continuidade da importação.
A Anvisa já aprovou para uso no Brasil a CoronaVac, a vacina de Oxford/AstraZeneca, a da Pfizer/BioNTech e a da Johnson & Johnson. Esta última, entretanto, ainda não tem doses disponíveis no país.
Mas as doses importadas poderão ser usadas?
Sim, pelo que estabelece o parágrafo 3º, do art. 13 da lei 14.124/2021:
§ 3º Os Estados, os Municípios e o Distrito Federal ficam autorizados a adquirir, a distribuir e a aplicar as vacinas contra a Covid-19 registradas, autorizadas para uso emergencial ou autorizadas excepcionalmente para importação, nos termos do art. 16 desta Lei, caso a União não realize as aquisições e a distribuição tempestiva de doses suficientes para a vacinação dos grupos previstos no Plano Nacional de Operacionalização da Vacinação contra a Covid-19.
A área técnica da Anvisa impôs algumas restrições ao uso dos imunizantes.
Veja Mais em G1 Globo
Confira notícias de Foz do Iguaçu no Facebook do Diário de Foz e no Instagram do Diário de Foz